Công thức LEWIS là gì? cách viết công thức LEWIS và ví dụ minh hoạ - Hỏi đáp Hoá 10 Chân trời sáng tạo
Công thức Lewis biểu diễn sự hình thành liên kết hoá học giữa các nguyên tử trong một phân tử.
Công thức Lewis của một phần tử được xây dựng từ công thức electron của phân tử, trong đó mỗi cặp electron chung giữa hai nguyên tử tham gia liên kết được thay bằng một gạch nối "-".
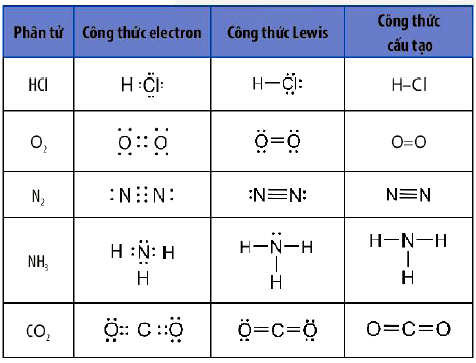 Công thức electron, công thức Lewis và công thức cấu tạo của một số phân tử
Công thức electron, công thức Lewis và công thức cấu tạo của một số phân tử
Ví dụ: Viết công thức Lewis của SO2, SO3, N2, NO2, HNO3, H2S, SF6, C2H2...
* Công thức Lewis của SO3
+ Bước 1: S có 6 electron hóa trị, O có 6 electron hóa trị. Trong phân tử SO3, có 1 nguyên tử S và 3 nguyên tử O
⇒ Tổng số electron hóa trị là: 1.6 + 3.6 = 24 electron
+ Bước 2: Sơ đồ khung biểu diễn liên kết của phân tử SO3
S có độ âm điện nhỏ hơn nên S là nguyên tử trung tâm.
![]()
+ Bước 3: Số electron hóa trị chưa tham gia liên kết trong sơ đồ là: 24 – 2.3 = 18 electron
Hoàn thiện octet cho nguyên tử có độ âm điện lớn hơn trong sơ đồ:
Sử dụng 18 electron này để tạo octet cho O trước (vì O có độ âm điện cao hơn)
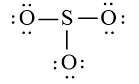
+ Bước 4: Đã sử dụng hết 18 electron để tạo octet cho O. Tuy nhiên S chưa đủ octet nên ta chuyển 1 cặp electron của nguyên tử O tạo thành cặp electron dùng chung.
Công thức Lewis của SO3 là:
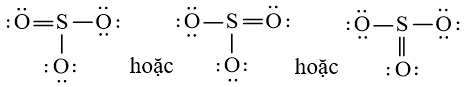
* Công thức Lewis của N2
+ Bước 1. Số electron hóa trị là 5.2 = 10 electron
+ Bước 2. Trong phân tử N2, mỗi nguyên tử N cần 3 electron để đạt octet.
![]()
+ Bước 3. Mỗi nguyên tử N cần 6 electron hóa trị để đạt octet:
![]()
+ Bước 4. Số electron hóa trị còn lại là: 10 – 6.2 – 2.1 = - 4
- Số electron hóa trị của nguyên tử N là 5, nên để đạt octet mỗi nguyên tử N sẽ góp chung 3 electron hóa trị để tạo liên kết với nhau.
Công thức Lewis của phân tử N2 là:
![]()
* Công thức Lewis của SO2
+ Bước 1. Số electron hóa trị là 1.6 + 2.6 = 18 electron.
+ Bước 2. Trong phân tử SO2, nguyên tử S cần 2 electron để đạt octet, nguyên tử O cần 2 electron hóa trị để đạt octet. Vì vậy, S là nguyên tử trung tâm, còn nguyên tử O được xếp xung quanh:
![]()
+ Bước 3. Hoàn thiện octet cho nguyên tử O:
![]()
+ Bước 4. Số electron hóa trị còn lại: 18 – 2.2 – 2.6 = 2
Sử dụng 2 electron này để tạo octet cho S.
Nguyên tử S có 4 electron hóa trị nên 1 nguyên tử O sẽ dùng 1 cặp electron để tạo liên kết với S và nguyên tử S còn 1 đôi electron chưa tham gia liên kết.
Công thức Lewis của SO2 là:
![]()
» Hãy xem để hiểu thêm về cách viết cấu trúc Lewis
| Công thức Lewis của: | ||||
| SO2 | SO3 | N2 | NH3 | NO2 |
| HNO3 | H2SO4 | CH4 | H3PO4 | HBr |
| H2CO3 | H2SO3 | HCl | H2S | C2H4 |
| C2H2 | CO2 | CO | NO | N2O3 |
| H3O+ | NO3- | PCl3 | P2O5 | Cl2O7 |
| Cl2 | H2 | O2 | H2O2 | H2O |
| CH3CHO | CH3COOH | CH3OH | SCl2 | CS2 |
| CCl4 | BF3 | BH3 | F2O | SF6 |
| SF4 | PCl5 | SO32- | NH4+ | NCl3 |
| N2O4 | N2O5 | HClO3 | HClO4 | HClO |
| HClO2 | ||||
Trên đây KhoiA.Vn đã hướng dẫn các em giải đáp thắc mắc về Công thức Lewis là gì? Cách viết công thức Lewis và một số ví dụ minh hoạ trong nội dung Hoá 10 Chân trời sáng tạo. Nếu có câu hỏi hay góp ý các em hãy để lại bình luận dưới bài viết nhé, chúc các em thành công.
» Xem thêm: Lý thuyết Hoá 10 Chân trời sáng tạo
» Lý thuyết Hóa 10 Bài 1: Nhập môn hóa học
» Lý thuyết Hóa 10 Bài 2: Thành phần của nguyên tử
» Lý thuyết Hóa 10 Bài 3: Nguyên tố hóa học
» Lý thuyết Hóa 10 Bài 4: Cấu trúc lớp vỏ electron của nguyên tử
» Lý thuyết Hóa 10 Bài 5: Cấu tạo bảng tuần hoàn các nguyên tố...
» Lý thuyết Hóa 10 Bài 6: Xu hướng biến đổi một số tính chất...
» Lý thuyết Hóa 10 Bài 7: Định luật tuần hoàn – ý nghĩa ....
» Lý thuyết Hóa 10 Bài 8: Quy tắc octet
» Lý thuyết Hóa 10 Bài 9: Liên kết ion
» Lý thuyết Hóa 10 Bài 10: Liên kết cộng hóa trị
» Lý thuyết Hóa 10 Bài 11: Liên kết hydrogen và tương tác van der waals
» Lý thuyết Hóa 10 Bài 12: Phản ứng oxi hóa – khử và ứng dụng trong...
» Lý thuyết Hóa 10 Bài 13: Enthalpy tạo thành và biến thiên enthalpy...
» Lý thuyết Hóa 10 Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
» Lý thuyết Hóa 10 Bài 15: Phương trình tốc độ phản ứng và hằng số...
» Lý thuyết Hóa 10 Bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
» Lý thuyết Hóa 10 Bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA
» Lý thuyết Hóa 10 Bài 18: Hydrogen halide và một số phản ứng của ion halide
Đánh giá & nhận xét
- Tìm m để đường thẳng tiếp xúc với đường tròn Toán 10 - Hỏi nhanh đáp gọn
- Đơn vị Micro, Nano, Pico? Bảng mẫu đơn vị về ước số và bội số trong SI? Hỏi đáp môn Vật lí
- Hệ đơn vị SI là gì? 7 đơn vị cơ bản của hệ SI? Hỏi nhanh đáp gọn môn Vật lí
- Giải hệ phương trình bằng quy tắc Cramer, Phương pháp định thức Cramer lớp 10
- Phương trình bậc 2 có đúng 1 nghiệm dương khi nào? Điều kiện PT bậc 2 có đúng 1 nghiệm dương - Toán lớp 10
- Giải Vật lí 10 trang 92 Chân trời Sáng tạo
- Giải Vật lí 10 trang 91 Chân trời Sáng tạo
- Giải Vật lí 10 trang 90 Chân trời Sáng tạo
- Giải Vật lí 10 trang 89 Chân trời Sáng tạo
- Giải Vật lí 10 trang 88 Chân trời Sáng tạo


































