Ảnh hưởng của nồng độ, nhiệt độ, áp suất, bề mặt tiếp xúc và chất xúc tác tới tốc độ phản ứng và ví dụ - Hoá 10 bài 16
Các yêu tố ảnh hưởng đến tốc độ phản ứng là nội dung bài 16 Hoá 10 SGK Chân trời sáng tạo. Sau đây là tóm tắt ngắn gọn, đầy đủ và dễ hiểu bài Các yêu tố ảnh hưởng đến tốc độ phản ứng để các em thuận tiện tham khảo.
Bài này sẽ giúp các em hiểu rõ về các yếu tố ảnh hưởng đến tốc độ phản ứng đó là: Ảnh hưởng của nồng độ, nhiệt độ, áp suất, bề mặt tiếp xúc và chất xúc tác.
1. Ảnh hưởng của nồng độ tới tốc độ phản ứng
- Khi tăng nồng độ chất phản ứng, tốc độ phản ứng tăng.
- Giải thích: Nồng độ của các chất phản ứng tăng làm tăng số va chạm hiệu quả nên tốc độ phản ứng tăng.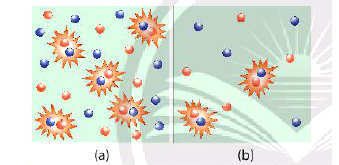
Ảnh hưởng của nồng độ tới tốc độ phản ứng Hoá 10 bài 16
> Lưu ý: Khi các chất phản ứng va chạm đúng hướng và đủ năng lượng dẫn đến xảy ra phản ứng, gọi là va chạm hiệu quả.
* Ví dụ: Phản ứng hóa học: Na2S2O3(aq) + H2SO4(aq) → Na2SO4(aq) + S(s) + SO2(g) + H2O(l)
Nồng độ Na2S2O3 giảm ⇒ Các hạt phân tử Na2S2O3 giảm
⇒ Số va chạm hiệu quả giữa các phân tử Na2S2O3 và phân tử H2SO4 giảm
⇒ Kết tủa tạo thành chậm tức là tốc độ phản ứng chậm hơn.
2. Ảnh hưởng của nhiệt độ tới tốc độ phản ứng
- Khi tăng nhiệt độ, tốc độ phản ứng tăng.
- Giải thích: Ở nhiệt độ thường, các chất phản ứng chuyển động với tốc độ nhỏ; khi tăng nhiệt độ; các chất sẽ chuyển động với tốc độ lớn hơn, dẫn đến tăng số va chạm hiệu quả nên tốc độ phản ứng tăng.
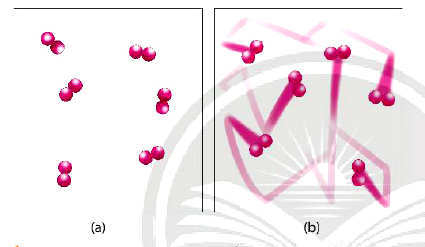
Ảnh hưởng của nhiệt độ tới tốc độ của phản ứng
- Mối quan hệ giữa nhiệt độ và tốc độ phản ứng hóa học được biểu diễn bằng công thức:
Trong đó:
vt1; vt2 là tốc độ phản ứng ở hai nhiệt độ t1 và t2;
γ là hệ số nhiệt độ Van't Hoff.
> Lưu ý: Quy tắc Van't Hoff chỉ gần đúng trong khoảng nhiệt độ không cao.
3. Ảnh hưởng của áp suất tới tốc độ phản ứng
- Đối với phản ứng có chất khí tham gia, tốc độ phản ứng tăng khi tăng áp suất.
- Giải thích: Khi tăng áp suất thì nồng độ chất khí tăng, nên tốc độ phản ứng tăng.

Ảnh hưởng của áp suất tới tốc độ phản ứng (tốc độ phản ứng tăng khi tăng áp suất)
4. Ảnh hưởng của bề mặt tiếp xúc
- Khi tăng diện tích bề mặt tiếp xúc của chất phản ứng, tốc độ phản ứng tăng.
- Giải thích: Khi tăng diện tích tiếp xúc của chất phản ứng, số va chạm hiệu quả tăng dẫn đến tốc độ phản ứng tăng.
* Ví dụ: Thực hiện các thí nghiệm sau:
+ Thí nghiệm 1: Cho 2 gam CaCO3 dạng khối tác dụng với 20 ml HCl 1M;
+ Thí nghiệm 2: Cho 2 gam CaCO3 dạng bột tác dụng với 20 ml HCl 1M.
Khi HCl phản ứng với CaCO3 dạng bột, diện tích tiếp xúc giữa các phân tử HCl và CaCO3 tăng lên
⇒ Số va chạm hiệu quả tăng
⇒ tốc độ phản ứng tăng.
⇒ Ở thí nghiệm 2 phản ứng diễn ra nhanh hơn.
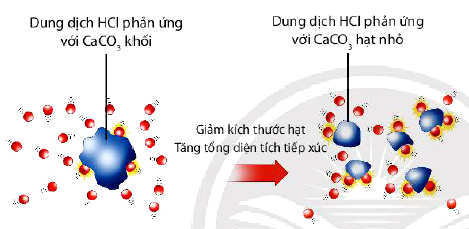
Ảnh hưởng của bề mặt tiếp xúc tới tốc độ phản ứng
5. Ảnh hưởng của chất xúc tác tới tốc độ phản ứng
- Chất xúc tác làm tăng tốc độ của phản ứng hóa học, nhưng vẫn được bảo toàn về lượng và chất khi kết thúc phản ứng.
- Chất xúc tác được ghi trên mũi tên trong phương trình hóa học.
* Ví dụ 1: Phương trình hóa học của phản ứng:
2H2O2 (aq) 2H2O (l) + O2 (g)
Trong phản ứng trên MnO2 là chất xúc tác.
* Ví dụ 2: Enzyme amylase có trong nước bọt là chất xúc tác đẩy nhanh quá trình tiêu hóa tinh bột.
6. Ý nghĩa thực tiễn của tốc độ phản ứng trong đời sống và sản xuất
- Kiểm soát tốc độ các phản ứng diễn ra trong đời sống, sản xuất khi vận dụng các yếu tố ảnh hưởng như: nồng độ, nhiệt độ, áp suất, bề mặt tiếp xúc và chất xúc tác giúp mang lại các giá trị hiệu quả.

Ý nghĩa thực tiễn của tốc độ phản ứng trong đời sống và sản xuất
* Ví dụ:
- Nồng độ oxygen trong không khí chỉ chiếm 21%. Dùng bình chứa oxygen mục đích làm tăng nồng độ chất tham gia
⇒ Tăng tốc độ phản ứng cháy
- Bảo quản thức ăn trong tủ lạnh ⇒ Giảm nhiệt độ
⇒ Giảm tốc độ phản ứng oxi hóa thức ăn
⇒ Thức ăn lâu bị ôi thiu.
Trên đây KhoiA.Vn đã giới thiệu với các em về Ảnh hưởng của nồng độ, nhiệt độ, áp suất, bề mặt tiếp xúc và chất xúc tác tới tốc độ phản ứng và ví dụ - Hóa 10 bài 16 SGK Chân trời sáng tạo. Nếu có câu hỏi hay góp ý các em hãy để lại bình luận dưới bài viết nhé, chúc các em thành công.
® Lý thuyết Hoá 10 Sách giáo khoa (SGK) Chân trời sáng tạo có thể bạn muốn xem
» Bài 2: Thành phần của nguyên tử
» Bài 4: Cấu trúc lớp vỏ electron của nguyên tử
» Bài 5: Cấu tạo bảng tuần hoàn các nguyên tố hóa học
» Bài 7: Định luật tuần hoàn – ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
» Bài 10: Liên kết cộng hóa trị
» Bài 11: Liên kết hydrogen và tương tác van der waals
» Bài 12: Phản ứng oxi hóa – khử và ứng dụng trong cuộc sống
» Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
» Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
» Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
» Bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA
» Bài 18: Hydrogen halide và một số phản ứng của ion halide
• Xem hướng dẫn giải bài tập SGK Hoá 10 Chân trời sáng tạo
Đánh giá & nhận xét
- Tìm m để đường thẳng tiếp xúc với đường tròn Toán 10 - Hỏi nhanh đáp gọn
- Đơn vị Micro, Nano, Pico? Bảng mẫu đơn vị về ước số và bội số trong SI? Hỏi đáp môn Vật lí
- Hệ đơn vị SI là gì? 7 đơn vị cơ bản của hệ SI? Hỏi nhanh đáp gọn môn Vật lí
- Giải hệ phương trình bằng quy tắc Cramer, Phương pháp định thức Cramer lớp 10
- Phương trình bậc 2 có đúng 1 nghiệm dương khi nào? Điều kiện PT bậc 2 có đúng 1 nghiệm dương - Toán lớp 10
- Giải Vật lí 10 trang 92 Chân trời Sáng tạo
- Giải Vật lí 10 trang 91 Chân trời Sáng tạo
- Giải Vật lí 10 trang 90 Chân trời Sáng tạo
- Giải Vật lí 10 trang 89 Chân trời Sáng tạo
- Giải Vật lí 10 trang 88 Chân trời Sáng tạo




































