Phát biểu nội dung Định luật bảo toàn Khối lượng Công thức tính của định luật bảo toàn khối lượng - Hóa 8 bài 15
Định luật bảo toàn khối lượng là một trong những định luật quan trọng mà các em được học trong chương trình hóa học lớp 8, đây là nội dung nền tảng trong nhiều phương pháp giải các bài tập về hóa học.
Bài viết này giúp các em biết nội dung của định luật bảo toàn khối lượng phát biểu như thế nào? Định luật bảo toàn khối lượng có công thức ra sao? thí nghiệm của định luật bảo toàn khối lượng và vận dụng.
» Bài tập Định luật bảo toàn khối lượng: Giải bài 1, 2, 3 trang 54 SGK Hóa 8 bài 15
I. Thí nghiệm định luật bảo toàn khối lượng
• Bố trí thí nghiệm như sau:
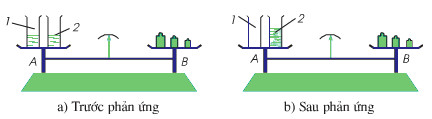 Phản ứng hóa học trong cốc trên đĩa cân
Phản ứng hóa học trong cốc trên đĩa cân
• Thực hiện thí nghiệm như sau:
- Đặt 2 cốc chứa dd BaCl2 và Na2SO4 lên 1 đĩa cân
- Đặt các quả cân lên đĩa cân còn lại.
- Đổ cốc đựng dung dịch BaCl2 vào cốc đựng dung dịch Na2SO4
• Quan sát thấy, có chất màu trắng xuất hiện, đó là bari sunfat BaSO4, chất này không tan, đã xảy ra phản ứng hóa học sau:
Bari clorua + Natri sunfat → Bari sunfat + Natri clorua
• Kim cân ở vị trí thăng bằng.
II. Định luật bảo toàn khối lượng
• Định luật bảo toàn khối lượng do 2 nhà khoa học Lo-mô-nô-xốp (Người Nga, 1711-1765) và La-voa-diê (người Pháp, 1743-1794) phát hiện ra
• Phát biểu nội dung định luật bảo toàn khối lượng: Trong một phản ứng hóa học, tổng khối lượng các chất sản phẩm bằng tổng khối lượng các chất tham gia phản ứng.
> Lưu ý: Trong phản ứng hóa học liên kết giữa các nguyên tử bị thay đổi. Số nguyên tử của mỗi nguyên tố giữ nguyên và khối lượng của các nguyên tử không đổi (được bảo toàn).
III. Áp dụng định luật bảo toàn khối lượng
• Giả sử có phương trình phản ứng: A + B → C + D
• Công thức tính của định luật bảo toàn khối lượng như sau:
mA + mB → mC + mD
Trong đó: mA; mB; mC; mD là khối lượng của mỗi chất.
* Ví dụ, công thức về khối lượng của các chất phản ứng trong thí nghiệm là:
mBaCl2 + mNa2SO4 = mBaSO4 + mNaCl
• Trong công thức này, nếu biết khối lượng của 3 chất thì ta tính được khối lượng của chất còn lại.
Gọi a, b, c lần lượt là khối lượng của Bari Clorua, Natri Sunfat và Natri Clorua và x là số mol của Bari Sunfat.
Ta có: mBaCl2 + mNa2SO4 = mBaSO4 + mNaCl
⇔ a + b = c + x
⇒ x = a + b - c.
* Ví dụ: Cho 4g NaOH tác dụng với 8g CuSO4 tạo ra 4,9g Cu(OH)2 kết tủa và Na2SO4. Tính khối lượng Na2SO4.
* Lời giải:
Áp dụng ĐLBT khối lượng, ta có:
mNaOH + mCuSO4 = mCu(OH)2 + mNa2SO4
4 + 8 = 4,9 + mNa2SO4
Thay số, suy ra:
mNa2SO4 = 4 + 8 - 4,9 = 7,1(g)
Trên đây KhoiA.Vn đã giới thiệu với các em về nội dung định luật bảo toàn khối lượng, công thức tính của định luật bảo toàn khối lượng trong SGK Hóa học 8 nội dung bài 15. Hy vọng bài viết giúp các em hiểu rõ hơn. Nếu có câu hỏi hay góp ý các em hãy để lại bình luận dưới bài viết, chúc các em thành công.
Đánh giá & nhận xét
- Cách chứng minh 3 điểm thẳng hàng Toán lớp 8
- Phân tích đa thức thành nhân tử, 8 cách phân tích đa thức thành nhân tử và ví dụ minh hoạ Toán lớp 8
- Bài 1 trang 52 SGK Toán 8 Tập 1 Chân trời sáng tạo
- Phân tích đa thức thành nhân tử bằng phương pháp dùng Hằng Đẳng Thức - Toán 8 bài 7
- Cách nhân đơn thức với đa thức (Quy tắc nhân đơn thức đa thức) - Toán 8 bài 1
- Bất phương trình một ẩn là gì? Cách tìm tập nghiệm của bất phương trình - Toán 8 tập 2 bài 3
- Cách nhân đa thức với đa thức (Quy tắc nhân đa thức với đa thức) - Toán 8 bài 2 tập 1
- Bài tập nhân Đa thức với Đa thức - Toán 8 bài 2 tập 1
- Các hằng đẳng thức đáng nhớ: Bình phương của một tổng, một hiệu và hiệu hai bình phương - Toán 8 bài 3 tập 1
- Bài tập về các hằng đẳng thức đáng nhớ: bình phương của một tổng, một hiệu và hiệu hai bình phương - Toán 8 bài 3 tập 1


































