Bài 4 trang 54 SGK Hoá 10 Chân trời sáng tạo
Giải thích sự hình thành liên kết trong phân tử H2O bằng cách áp dụng quy tắc octet.
Bài 4 trang 54 SGK Hoá 10 Chân trời sáng tạo: Giải thích sự hình thành liên kết trong phân tử H2O bằng cách áp dụng quy tắc octet.
Giải bài 4 trang 54 SGK Hoá 10 Chân trời sáng tạo:
- Nguyên tử O (Z = 8): 1s22s22p4
⇒ Có 6 electron lớp ngoài cùng
⇒ Có xu hướng nhận 2 electron để đạt được cấu hình electron giống khí hiếm.
- Nguyên tử H (Z = 1): 1s1
⇒ Có xu hướng nhận 1 electron để đạt được cấu hình electron giống khí hiếm.
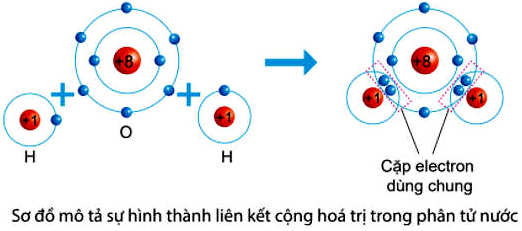
⇒ Mỗi nguyên tử H sẽ góp chung 1 electron với nguyên tử O (góp chung 2 electron) tạo thành 2 cặp electron dùng chung
Trên đây KhoiA.Vn đã hướng dẫn các em giải bài 4 trang 54 SGK Hoá 10 Chân trời sáng tạo. Nếu có câu hỏi hay góp ý các em hãy để lại bình luận dưới bài viết nhé, chúc các em thành công.
• Xem hướng dẫn giải bài tập Hoá 10 Chân trời sáng tạo
® Lý thuyết Hoá 10 Sách giáo khoa (SGK) Chân trời sáng tạo có thể bạn muốn xem
» Bài 2: Thành phần của nguyên tử
» Bài 4: Cấu trúc lớp vỏ electron của nguyên tử
» Bài 5: Cấu tạo bảng tuần hoàn các nguyên tố hóa học
» Bài 7: Định luật tuần hoàn – ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
» Bài 10: Liên kết cộng hóa trị
» Bài 11: Liên kết hydrogen và tương tác van der waals
» Bài 12: Phản ứng oxi hóa – khử và ứng dụng trong cuộc sống
» Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
» Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
» Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
» Bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
» Bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA
Đánh giá & nhận xét
- Tìm m để đường thẳng tiếp xúc với đường tròn Toán 10 - Hỏi nhanh đáp gọn
- Đơn vị Micro, Nano, Pico? Bảng mẫu đơn vị về ước số và bội số trong SI? Hỏi đáp môn Vật lí
- Hệ đơn vị SI là gì? 7 đơn vị cơ bản của hệ SI? Hỏi nhanh đáp gọn môn Vật lí
- Giải hệ phương trình bằng quy tắc Cramer, Phương pháp định thức Cramer lớp 10
- Phương trình bậc 2 có đúng 1 nghiệm dương khi nào? Điều kiện PT bậc 2 có đúng 1 nghiệm dương - Toán lớp 10
- Giải Vật lí 10 trang 92 Chân trời Sáng tạo
- Giải Vật lí 10 trang 91 Chân trời Sáng tạo
- Giải Vật lí 10 trang 90 Chân trời Sáng tạo
- Giải Vật lí 10 trang 89 Chân trời Sáng tạo
- Giải Vật lí 10 trang 88 Chân trời Sáng tạo




































