Công thức Lewis của PO43- (PO43- Lewis Structure)
Chi tiết hướng dẫn cách viết công thức Lewis của PO43-, công thức electron, công thức cấu tạo của các nguyên tố hóa học theo SGK mới dễ hiểu.
Sau đây là cách viết công thức Lewis của PO43- (PO43- lewis structure) được hướng dẫn cụ thể, chi tiết từng bước và dễ hiểu để các bạn tham khảo.
Viết công thức Lewis của PO43- (theo công thức phân tử và electron hoá trị)
Thực hiện lần lượt theo các bước sau:
• Bước 1: Tính tổng số electron hóa trị trong phân tử
P có 5 electron hóa trị, O có 6 electron hóa trị. Trong phân tử PO43-, có 1 nguyên tử P và 4 nguyên tử O.
Vậy tổng số electron hóa trị = 5.1 + 6.4 + 3 = 32 electron.
• Bước 2: Vẽ khung phân tử tạo bởi liên kết đơn giữa các nguyên tử
Trong phân tử PO43-, nguyên tử P là nguyên tử trung tâm, các nguyên tử O được xếp xung quanh như sau:
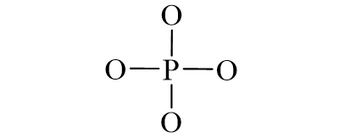
• Bước 3: Tính số electron hóa trị chưa tham gia liên kết bằng cách lấy tổng số electron trừ số electron tham gia tạo liên kết.
Số electron hóa trị chưa tham gia liên kết trong sơ đồ là:
32 – 2.4 = 24 electron.
Sử dụng 24 electron này để tạo octet cho 4 nguyên tử O.
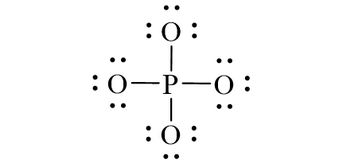
Đã sử dụng hết 24 electron để tạo octet cho 4 nguyên tử O.
Vậy công thức Lewis của PO43- là
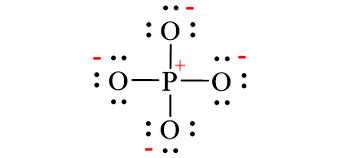
Tuy nhiên công thức trên không bền, do nguyên tử P và nguyên tử O đều mang điện tích, và điện tích càng lớn thì càng kém bền.
• Bước 4: Chuyển cặp electron chưa liên kết trên nguyên tử xung quanh thành electron liên kết sao cho hợp chất trở nên bền vững.
Ta chuyển 1 cặp electron của nguyên tử O vừa được tạo octet tạo thành cặp electron dùng chung với nguyên tử P. Điện tích đã không còn ở nguyên tử P và 1 nguyên tử O. Vì vậy, công thức trên bền hơn.
Vậy công thức Lewis của PO43- là
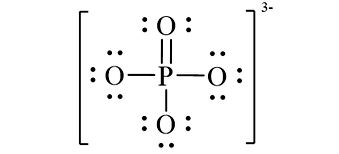
» Hãy xem để hiểu thêm về cách viết cấu trúc Lewis
| Công thức Lewis của: | ||||
| SO2 | SO3 | N2 | NH3 | NO2 |
| HNO3 | H2SO4 | CH4 | H3PO4 | HBr |
| H2CO3 | H2SO3 | HCl | H2S | C2H4 |
| C2H2 | CO2 | CO | NO | N2O3 |
| H3O+ | NO3- | PCl3 | P2O5 | Cl2O7 |
| Cl2 | H2 | O2 | H2O2 | H2O |
| CH3CHO | CH3COOH | CH3OH | SCl2 | CS2 |
| CCl4 | ||||
Trên đây KhoiA.Vn đã hướng dẫn các em Cách viết công thức Lewis của PO43- (PO43- lewis structure) Nếu có câu hỏi hay góp ý các em hãy để lại bình luận dưới bài viết nhé, chúc các em thành công.
Đánh giá & nhận xét
- Tìm m để đường thẳng tiếp xúc với đường tròn Toán 10 - Hỏi nhanh đáp gọn
- Đơn vị Micro, Nano, Pico? Bảng mẫu đơn vị về ước số và bội số trong SI? Hỏi đáp môn Vật lí
- Hệ đơn vị SI là gì? 7 đơn vị cơ bản của hệ SI? Hỏi nhanh đáp gọn môn Vật lí
- Giải hệ phương trình bằng quy tắc Cramer, Phương pháp định thức Cramer lớp 10
- Phương trình bậc 2 có đúng 1 nghiệm dương khi nào? Điều kiện PT bậc 2 có đúng 1 nghiệm dương - Toán lớp 10
- Giải Vật lí 10 trang 92 Chân trời Sáng tạo
- Giải Vật lí 10 trang 91 Chân trời Sáng tạo
- Giải Vật lí 10 trang 90 Chân trời Sáng tạo
- Giải Vật lí 10 trang 89 Chân trời Sáng tạo
- Giải Vật lí 10 trang 88 Chân trời Sáng tạo


































