Tính chất vật lý của nhôm (Al), tính chất hóa học của nhôm, cách sản xuất nhôm và ứng dụng - Hóa 9 bài 18
Nhôm và hợp kim nhôm được sử dụng rộng rãi trong đời sống như làm đồ dùng gia đình (xoong, chảo, ấm đun nước,...); dây dẫn điện; vật liệu xây dựng;...
Bài viết này sẽ giới thiệu tới các em về tính chất vật lý, tính chất hóa học của nhôm (Al); cách sản xuất nhôm và các ứng dụng của nhôm trong đời sống.
» Giải bài tập Hóa 9 bài 18: Giải bài 1, 2, 3, 4, 5, 6 trang 57, 58 SGK Hóa 9 bài 18
- Ký hiệu hóa học của nhôm: Al
- Nguyên tử khối của nhôm: 27
Tính chất hóa học của nhôm Al:
- Tác dụng với phi kim (O2, Cl2, S,...)
- Tác dụng với dung dịch axit (HCl, H2SO4 loãng,...)
- Tác dụng với muối của kim loại yếu hơn (CuCl2, AgNO3,...)
- Tác dụng với dung dịch kiềm (NaOH, KOH,...)
I. Tính chất vật lý của nhôm Al
- Nhôm là kim loại màu trắng bạc có ánh kim, nhẹ (khối lượng riêng: D = 2,7 g/cm3). Nhôm có tính dẻo, dẫn điện và dẫn nhiệt tốt, nóng chảy ở 660°C.
- Nhôm có tính dẻo nên dẽ cán mỏng hoặc kéo thành sợi.
II. Tính chất hóa học của nhôm Al
1. Nhôm có tính chất hóa học của một kim loại
a) Phản ứng của nhôm với phi kim
• Nhôm tác dụng với oxi tạo thành oxit nhôm:
4Al + 3O2 2Al2O3
- Ở điều kiện thường, nhôm phản ứng với oxi tạo thành lớp Al2O3 mỏng bền vững, lớp oxit này bảo vệ đồ vật bằng nhôm, không cho nhôm tác dụng oxi trong không khí, nước.
• Nhôm tác dụng với phi kim khác tạo thành muối (Cl2, S,..)
- Ở nhiệt độ thường, nhôm tác dụng với khí Clo tạo thành muối nhôm clorua
2Al + 3Cl2 → 2AlCl3
b) Nhôm phản ứng với dung dịch axit
- Nhôm tác dụng với một số dung dịch axit như HCl, H2SO4 loãng,... tạo thành muối và giải phóng khí hidro
2Al + 6HCl → 2AlCl3 + 3H2
> Lưu ý: Nhôm không tác dụng với H,SO4, HNO3 đặc, nguội.
c) Phản ứng của nhôm với dung dịch muối
- Nhôm phản ứng với nhiều dung dịch muối của những kim loại yếu hơn (hoạt động hóa học yếu hơn) tạo ra muối nhôm và kim loại mới.
2Al + 3CuCl2 → 2AlCl3 + 3Cu
Al + 3AgNO3 → Al(NO3)3 + 3Ag
2. Tính chất hóa học riêng của nhôm Al
- Do lớp oxit nhôm bị hòa tan trong kiềm nên nhôm phản ứng với dung dịch kiềm.
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
III. Ứng dụng của nhôm
- Nhôm được ứng dụng làm đồ dùng gia đình, dây dẫn điện, vật liệu xây dựng,...
- Đuyra (hợp kim của nhôm với đồng và một số nguyên tố khác như mangan, sắt, silic) nhẹ và bền nên được dùng trong chế tạo máy bay, ô tô, tàu vũ trụ,...
IV. Sản xuất nhôm
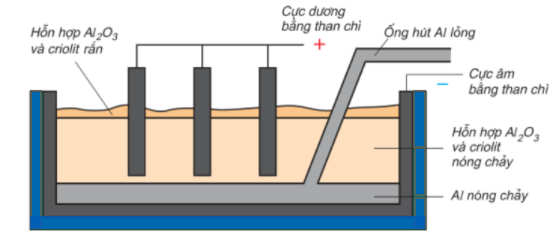
- Nguyên liệu để sản xuất nhôm là quặng bôxit có thành phần chủ yếu là Al2O3. Sau khi đã loại bỏ tạp chất, rigười ta điện phân Al2O3 nóng chảy (có pha thêm chất criolit có tác dụng làm giảm nhiệt dộ nóng chảy của nhôm oxit), thu được nhôm.
2Al2O3 4Al + 3O2
Trên đây KhoiA.Vn đã giới thiệu với các em về Tính chất vật lý của nhôm (Al), tính chất hóa học của nhôm, cách sản xuất nhôm và ứng dụng. Hy vọng bài viết giúp các em hiểu rõ hơn. Nếu có câu hỏi hay góp ý các em hãy để lại bình luận dưới bài viết, chúc các em thành công.
Đánh giá & nhận xét
- Tìm giá trị nhỏ nhất, giá trị lớn nhất của tam thức bậc 2
- Tìm giá trị nhỏ nhất, giá trị lớn nhất của biểu thức chứa trị tuyệt đối
- Tìm giá trị nhỏ nhất (gtnn), giá trị lớn nhất (gtln) của biểu thức lớp 9
- Tìm giá trị nhỏ nhất, giá trị lớn nhất của biểu thức chứa dấu căn
- Cách chứng minh 3 điểm thẳng hàng Toán lớp 9
- Cách giải phương trình chứa ẩn ở mẫu lớp 9, phương trình chứa ẩn ở mẫu là gì?
- Cách giải phương trình tích lớp 9, phương trình tích là gì?
- Đường thẳng cắt parabol tại 2 điểm khi nào? Tìm m để d cắt P tại hai điểm thỏa điều kiện
- Số tiếp tuyến chung của hai đường tròn cắt nhau, ở ngoài nhau, tiếp xúc ngoài, tiếp xúc trong?
- Hai đường tròn cắt nhau có bao nhiêu tiếp tuyến chung?


































