Bài tập luyện tập Các loại hợp chất vô cơ: Giải bài 1, 2, 3 trang 43 SGK Hóa 9 bài 13
Ở những bài trước các em đã được học về tính chất hóa học của hợp chất vô cơ cũng như cách phân loại các hợp chất vô cơ.
Bài viết này nhằm củng cố các kiến thức đã học về cách phân loại và tính chất hóa học của các loại hợp chất vô cơ và giải một số bài tập vận dụng.
I. Kiến thức về các loại hợp chất vô cơ cần nhớ
1. Cách phân loại các hợp chất vô cơ
• Bảng dưới đây cho chúng ta biết về hệ thống phân loại các hợp chất vô cơ:
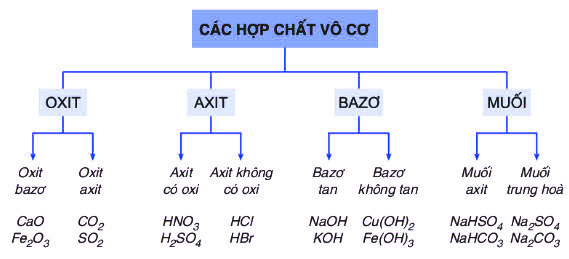
Bảng phân loại các loại hợp chất vô cơ
2. Tính chất hóa học của các loại hợp chất vô cơ
• Tính chất hóa học của các hợp chất vô cơ được tóm tắt bằng sơ đồ sau:
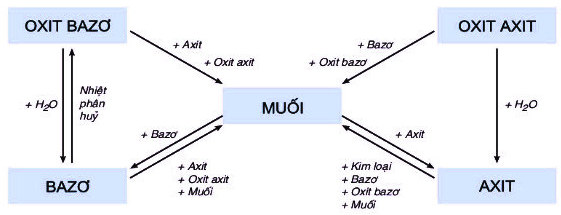
Tính chất hóa học của các hợp chất vô cơ
II. Giải bài tập 1, 2, 3 trang 43 SGK Hóa 9
* Bài 1 trang 43 SGK Hóa 9: Căn cứ vào sơ đồ biểu thị những tính chất hóa học của các hợp chất vô cơ:
1. Oxit
a) Oxit bazơ + ... → bazơ
b) Oxit bazơ + ... → muối + nước
c) Oxit axit + ... → axit
d) Oxit axit + ... → muối + nước
2. Bazơ
a) Bazơ + ... → muối + nước
b) Bazơ + ... → muối + nước
c) Bazơ + ... → muối + bazơ
d) Bazơ oxit bazơ + nước
e) Oxit axit + oxit bazơ → ...
3. Axit
a) Axit + ... → muối + hiđro
b) Axit + ... → muối + nước
c) Axit + ... → muối + nước
d) Axit + ... → muối + axit
4. Muối
a) Muối + ... → axit + muối
b) Muối + ... → muối + bazơ
c) Muối + ... → muối + muối
d) Muối + ... → muối + kim loại
e) Muối ... + ...
> Giải bài 1 trang 43 SGK Hóa 9
* Bài 2 trang 43 SGK Hóa 9: Để một mẩu natri hiđroxit trên tấm kính trong không khí, sau vài ngày thấy có chất rắn màu trắng phủ ngoài. Nếu nhỏ vài giọt dung dịch HCl vào chất rắn thấy có khí thoát ra, khí này làm đục nước vôi trong. Chất rắn màu trắng là sản phẩm phản ứng của natri hiđroxit với:
a) Oxit trong không khí.
b) Hơi nước trong không khí.
c) Cacbon đioxit và oxi trong không khí.
d) Cacbon đioxit và hơi nước trong không khí.
e) Cacbon đioxit trong không khí.
Giải thích và viết phương trình hóa học minh họa.
> Giải bài 2 trang 43 SGK Hóa 9
* Bài 3 trang 43 SGK Hóa 9: Trộn một dung dịch có hòa tan 0,2 mol CuCl2 với một dung dịch có hòa tan 20g NaOH. Lọc hỗn hợp các chất sau phản ứng, được kết tủa và nước lọc. Nung kết tủa đến khi khối lượng không đổi.
a) Viết các phương trình hóa học.
b) Tính khối lượng chất rắn thu được sau khi nung.
c) Tính khối lượng các chất có trong nước lọc.
Trên đây KhoiA.Vn đã hướng dẫn các em cách giải một số bài tập về Các loại hợp chất vô cơ: Giải bài 1, 2, 3 trang 43 SGK Hóa 9 bài 13. Hy vọng bài viết giúp các em hiểu rõ hơn. Nếu có câu hỏi hay góp ý các em hãy để lại bình luận dưới bài viết, chúc các em thành công.
Đánh giá & nhận xét
- Tìm giá trị nhỏ nhất, giá trị lớn nhất của tam thức bậc 2
- Tìm giá trị nhỏ nhất, giá trị lớn nhất của biểu thức chứa trị tuyệt đối
- Tìm giá trị nhỏ nhất (gtnn), giá trị lớn nhất (gtln) của biểu thức lớp 9
- Tìm giá trị nhỏ nhất, giá trị lớn nhất của biểu thức chứa dấu căn
- Cách chứng minh 3 điểm thẳng hàng Toán lớp 9
- Cách giải phương trình chứa ẩn ở mẫu lớp 9, phương trình chứa ẩn ở mẫu là gì?
- Cách giải phương trình tích lớp 9, phương trình tích là gì?
- Đường thẳng cắt parabol tại 2 điểm khi nào? Tìm m để d cắt P tại hai điểm thỏa điều kiện
- Số tiếp tuyến chung của hai đường tròn cắt nhau, ở ngoài nhau, tiếp xúc ngoài, tiếp xúc trong?
- Hai đường tròn cắt nhau có bao nhiêu tiếp tuyến chung?


































