Bài tập Axit Axetic CH3COOH: Giải bài 1, 2, 3, 4, 5, 6, 7, 8 trang 143 SGK Hóa 9
Các em đã tìm hiểu nội dung lý thuyết về trạng thái tự nhiên, tính chất vật lí, cấu tạo phân tử và tính chất hóa học của axit axetic (công thức cấu tạo viết gọn CH3COOH)
Dưới đây các em sẽ vận dụng các kiến thức về tính chất hóa học, cấu tạo phân tử và tính chất vật lí của axit AXETIC (công thức phân tử C2H4O công thức cấu tạo viết gọn CH3COOH) để giải một số bài tập cụ thể.
* Bài 1 trang 143 sgk hoá 9: Hãy điền những từ thích hợp vào các chỗ trống:
a) Axit axetic là chất ... không màu, vị ... tan ... trong nước.
b) Axit axetic là nguyên liệu để điều chế ...
c) Giấm ăn là dung dịch ... từ 2 đến 5%
d) Bằng cách ... butan với chất xúc tác thích hợp người ta thu được ...
* Lời giải bài 1 trang 143 sgk hoá 9:
a) Axit axetic là chất lỏng không màu, vị chua tan vô hạn trong nước.
b) Axit axetic là nguyên liệu để điều chế dược phẩm, phẩm nhuộm, chất dẻo, tơ nhân tạo.
c) Giấm ăn là dung dịch axit axetic có nồng độ từ 2 đến 5%
d) Bằng cách oxi hóa butan với chất xúc tác thích hợp người ta thu được axit axteic.
* Bài 2 trang 143 sgk hoá 9: Trong các chất sau đây:
a) C2H5OH.
b) CH3COOH.
c) CH3CH2CH2OH.
d) CH3CH2COOH.
Chất nào tác dụng được với Na, NaOH, Mg, CaO? Viết các phương trình hóa học.
* Lời giải bài 2 trang 143 sgk hoá 9:
- Chất tác dụng với Na là: a, b, c, d (do có gốc OH).
- Chất tác dụng với NaOH là: b, d (do có gốc COOH).
- Chất tác dụng với Mg là: b, d (do có gốc COOH).
- Chất tác dụng với CaO là: b, d (do có gốc COOH).
* Phương trình phản ứng hóa học:
2C2H5OH + 2Na → 2C2H5ONa + H2↑
2CH3COOH + 2Na → 2CH3COONa + H2↑
2C3H7OH + 2Na → 2C3H7ONa + H2↑
2C2H5COOH + 2Na → 2C2H5COONa + H2↑
CH3COOH + NaOH → CH3COONa + H2O
C2H5COOH + NaOH → C2H5COONa + H2O
2CH3COOH + Mg → (CH3COO)2Mg + H2↑
2C2H5COOH + Mg → (C2H5COO)2Mg + H2↑
2CH3COOH + CaO → (CH3COO)2Ca + H2O
2C2H5COOH + CaO → (C2H5COO)2Ca + H2O
* Bài 3 trang 143 sgk hoá 9: Axit axetic có tính axit vì trong phân tử
A. có 2 nguyên tử.
B. có nhóm -OH.
C. có nhóm -OH và =C=O.
D. có nhóm -OH kết hợp với nhóm =C=O tạo thành nhóm -COOH.
* Lời giải bài 3 trang 143 sgk hoá 9:
- Đáp án: D. có nhóm -OH kết hợp với nhóm =C=O tạo thành nhóm -COOH.
Câu D đúng vì trong phân tử axit axetic có nhóm -COOH.
* Bài 4 trang 143 sgk hoá 9: Trong các chất sau đây, chất nào có tính axit? Giải thích
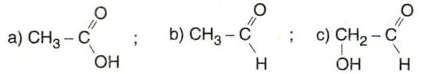
* Lời giải bài 4 trang 143 sgk hoá 9:
- Chất có tính axit là a) vì trong phân tử có nhóm – COOH.
(2 chất còn lại có nhóm anđehit -CHO)
* Bài 5 trang 143 sgk hoá 9: Axit axetic có thể tác dụng được với những chất nào trong các chất sau đây: ZnO, Na2SO4, KOH, Na2CO3, Cu, Fe? Viết các phương trình hóa học xảy ra (nếu có).
* Lời giải bài 5 trang 143 sgk hoá 9:
- Các chất tác dụng được với axit axetic là ZnO, KOH, Na2CO3, Fe.
- Phương trình hoá học phản ứng:
2CH3COOH + ZnO → (CH3COO)2Zn + H2O.
CH3COOH + KOH → CH3COOK + H2O.
2CH3COOH + Na2CO3 → 2CH3COONa + CO2↑ + H2O.
2CH3COOH + Fe → (CH3COO)2Fe + H2↑.
* Bài 6 trang 143 sgk hoá 9: Hãy viết phương trình hóa học điều chế axit axetic từ:
a) Natri axetic và axit sunfuric.
b) Rượu etylic.
* Lời giải bài 6 trang 143 sgk hoá 9:
Phương trình phản ứng điều chế axit axetic:
a) Từ natri axetic và axit sunfuric:
2CH3COONa + H2SO4 → 2CH3COOH + Na2SO4
b) Từ rượu etylic:
C2H5OH + O2 → CH3COOH + H2O.
* Bài 7 trang 143 sgk hoá 9: Cho 60 gam CH3-COOH tác dụng với 100g CH3-CH2-OH thu được 55gam CH3-COO-CH2-CH3
a) Viết phương trình hóa học xảy ra và gọi tên của phản ứng.
b) Tính hiệu suất của phản ứng trên
* Lời giải bài 7 trang 143 sgk hoá 9:
- Theo bài ra ta có:
nCH3COOH = 60/60 = 1 mol;
nC2H5OH = 100/46 = 2,17 mol.
a) Phương trình phản ứng:
CH3COOH + C2H5OH → CH3COOC2H5 + H2O
- Phản ứng này gọi là phản ứng este hóa.
b) Hiệu suất của phản ứng:
- Theo phương trình phản ứng trên và số liệu đề bài cho thì số mol rượu dư, do đó tính hiệu suất phản ứng theo CH3COOH.
- Theo lí thuyết 1 mol CH3COOH (60g) tạo ra 1 mol CH3COOC2H5 (88g) nhưng thực tế chỉ thu được 55g.
⇒ Vậy hiệu suất của phản ứng là: H% = (55/88).100% = 62,5%.
* Bài 8 trang 143 sgk hoá 9: Cho dung dịch axit axetic nồng độ a% tác dụng vừa đủ với dung dịch NaOH nồng độ 10% thu được dung dịch muối có nồng độ 10,25%. Hãy tính a.
* Lời giải bài 8 trang 143 sgk hoá 9:
- Gọi khối lượng dung dịch CH3COOH và NaOH cần dùng là m và m':
⇒ mCH3COOH = C%. mdd = m.a/100
⇒ nCH3COOH = (m.a)/(100.60)= (m.a)/6000 (mol).
- Tương tự: mNaOH = (m'.10)/100 = m'/10
⇒ nNaOH = m'/(40.10)= m'/400 (mol).
- Phương trình phản ứng:
CH3COOH + NaOH → CH3COONa + H2O.
- Theo phương trình phản ứng trên.
nCH3COOH = nNaOH = nCH3COONa.
Do đó ta có: m.a/6000 = m'/400 ⇒ a = (15.m')/m.
mCH3COONa = (82.m')/400 (g)
mdd sau pư = m + m’ (g)
Theo đề bài ta có: C% (CH3COONa) = ((82.m')/400)/(m + m') = 10,25/100.
Giải ra ta có m = m'. Thay vào a = (15.m')/m
⇒ a = 15.
⇒ Nồng độ dung dịch axit là 15%
Trên đây là nội dung phần Bài tập Axit Axetic CH3COOH: Giải bài 1, 2, 3, 4, 5, 6, 7, 8 trang 143 SGK Hóa 9. Nếu có góp ý, các em hãy để lại ở phần bình luận dưới bài viết để KhoiA.Vn ghi nhận, chúc các em thành công.
Đánh giá & nhận xét
- Tìm giá trị nhỏ nhất, giá trị lớn nhất của tam thức bậc 2
- Tìm giá trị nhỏ nhất, giá trị lớn nhất của biểu thức chứa trị tuyệt đối
- Tìm giá trị nhỏ nhất (gtnn), giá trị lớn nhất (gtln) của biểu thức lớp 9
- Tìm giá trị nhỏ nhất, giá trị lớn nhất của biểu thức chứa dấu căn
- Cách chứng minh 3 điểm thẳng hàng Toán lớp 9
- Cách giải phương trình chứa ẩn ở mẫu lớp 9, phương trình chứa ẩn ở mẫu là gì?
- Cách giải phương trình tích lớp 9, phương trình tích là gì?
- Đường thẳng cắt parabol tại 2 điểm khi nào? Tìm m để d cắt P tại hai điểm thỏa điều kiện
- Số tiếp tuyến chung của hai đường tròn cắt nhau, ở ngoài nhau, tiếp xúc ngoài, tiếp xúc trong?
- Hai đường tròn cắt nhau có bao nhiêu tiếp tuyến chung?


































