Amin là gì? Tính chất vật lý, Tính chất hóa học của Amin khái niệm và phân loại Amin - Hóa 12 bài 9
Amin là hợp chất được tạo thành khi thay thế một hay nhiều nguyên tử hiđro trong phân tử NH3 bằng một hay nhiều gốc hiđrocacbon.
Nội dung bài này sẽ giúp các em hiểu rõ amin là gì? Tính chất vật lý và tính chất hóa học của Amin, cách phân loại Amin.
I. Khái niệm, phân loại, danh pháp Amin
1. Khái niệm amin
- Khi thay thế một hay nhiều nguyên tử hiđro trong phân tử NH3 bằng một hay nhiều gốc hiđrocacbon ta được amin.
* Ví dụ: CH3–NH2 ; CH3–NH–CH3;
CH2=CH–CH2NH2; C6H5–NH2;
2. Phân loại amin
- Amin được phân loại theo đặc điểm cấu tạo của gốc hiđrocacbon (amin thơm, amin béo, amin dị vòng) và theo bậc của amin (amin bậc một, bậc hai, bậc ba)
> Lưu ý: Bậc của amin được tính bằng số gốc hidrocacbon liên kết trực tiếp với nguyên tử N
* Ví dụ: amin bậc 1: CH3CH2CH2-NH2
amin bậc 2: CH3CH2-NH-CH3
amin bậc 3: (CH3)3N
3. Danh pháp amin
• Amin bậc I (RNH2) có 2 cách gọi tên
Cách 1: Tên gốc hiđrocacbon + amin
Cách 2: Tên hiđrocacbon + số chỉ vị trí nhóm NH2 + amin
* Ví dụ: Tên gọi của một số amin
|
Hợp chất |
Tên gốc - chức |
Tên thay thế |
Tên thường |
|
CH3NH2 |
Metylamin |
Metanamin |
|
|
C2H5NH2 |
Etylamin |
Etanamin |
|
|
CH3CH2CH2NH2 |
Propylamin |
Propan - 1 – amin |
|
|
CH3CH(NH2)CH3 |
Isopropylamin |
Propan - 2 – amin |
|
|
H2N(CH2)6NH2 |
Hexametylenđiamin |
Hexan - 1,6 – điamin |
|
|
C6H5NH2 |
Phenylamin |
Benzenamin |
Anilin |
|
CH2=CH–CH2NH2 |
Anlylamin |
Prop-2-en-1-amin |
|
• Amin bậc II hoặc bậc III đọc theo tên gốc chức:
Tên gốc hiđrocacbon + amin
* Ví dụ: CH3–NH–C2H5 : Etylmetylamin
(CH3)3 –N : Trimetylamin
II. Tính chất vật lý của amin
- Metylamin, đimetylamin, trimetylamin và etylamin là những chất khí, mùi khai khó chịu, tan nhiều trong nước.
- Các chất đồng đẳng cao hơn là những chất lỏng hoặc rắn, độ tan trong nước giảm dần theo chiều tăng của phân tử khối.
- Anilin là chất lỏng, không màu, rất độc, ít tan trong nước, tan trong etanol, benzen.
III. Cấu tạo phân tử và tính chất hóa học của amin
1. Cấu tạo phân tử của amin
Trong phân tử amin, nguyên tử N tạo được một, hai hoặc ba liên kết với gốc hiđrocacbon, tương ứng có amin bậc một RNH2, amin bậc hai R-NH-R1, amin bậc ba: R-N(R2)-R1
Như vậy, Amin có tính bazơ và dễ bị oxi hóa tương tự NH3. Amin còn có tính chất của gốc hidrocacbon.
2. Tính chất hóa học của amin
a) Tính bazo của amin
- Dung dịch metylamin hoặc propylamin làm quỳ chuyển màu xanh, còn Anilin thì quỳ tím không đổi màu.
CH3CH2CH2NH2 + H2O [CH3CH2CH2NH3]+ + OH-
CH3NH2 + HCl → [CH3NH3]Cl (metylamoni clorua)
- Tính bazo của amin phụ thuộc mật độ electron trên nguyên tử N: Mật độ e lớn, tính bazơ mạnh:
Gốc hidrocacbon đẩy e làm tăng tính bazơ
Gốc hidrocacbon hút e làm giảm tính bazơ
Amin béo > NH3 > amin thơm
Amin béo bậc II > amin béo bậc I
b) Phản ứng thế ở nhân thơm của Anilin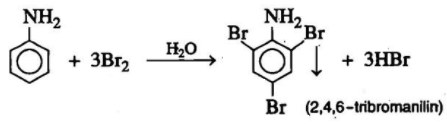
- Sản phẩm tạo ra kết tủa trắng nên đây là phản ứng đặc trưng dùng để nhận biết anilin với các amin khác
Trên đây KhoiA.Vn đã giới thiệu với các em về Amin là gì? Tính chất vật lý, Tính chất hóa học của Amin khái niệm và phân loại Amin. Hy vọng bài viết giúp các em hiểu rõ hơn. Nếu có câu hỏi hay góp ý các em hãy để lại bình luận dưới bài viết, chúc các em thành công.
• Xem hướng dẫn giải bài tập Hoá học 12
> Bài 2 trang 44 SGK Hóa 12: Có thể nhận biết lọ đựng CH3NH2 bằng cách nào sau đây?...
> Bài 5 trang 44 SGK Hóa 12: Hãy tìm phương pháp hóa học để giải quyết hai vấn đề sau:...
Đánh giá & nhận xét
- Cách chứng minh 3 vectơ KHÔNG đồng phẳng trong Oxyz lớp 12
- Cách tìm m để 3 vectơ đồng phẳng trong Oxyz lớp 12
- 3 vectơ đồng phẳng trong Oxyz khi nào, điều kiện 3 vectơ đồng phẳng lớp 12
- Viết phương trình parabol đi qua các điểm cực trị? Hỏi nhanh đáp gọn môn Toán
- Giải Địa lí 12 trang 23 Chân trời Sáng tạo
- Giải Địa lí 12 trang 27 Chân trời Sáng tạo
- Giải Địa lí 12 trang 26 Chân trời Sáng tạo
- Giải Địa lí 12 trang 25 Chân trời Sáng tạo
- Giải Địa lí 12 trang 22 Chân trời Sáng tạo
- Giải Địa lí 12 trang 21 Chân trời Sáng tạo


































