Cân bằng hóa học là gì? Các yếu tố ảnh hướng tới sự cân bằng hóa học, nguyên lý Le Chatelier - Hóa 10 bài 38
Các phản ứng hóa học đều thuộc một trong 2 dạng phản ứng: Phản ứng một chiều và phản ứng thuận nghịch.
Nội dung bài này sẽ giúp các em biết cân bằng hóa học là gì? Các yếu tố ảnh hưởng đến cân bằng hóa học và nguyên lý chuyển dịch cân bằng Le Chatelier.
I. Phản ứng một chiều, phản ứng thuận nghịch và cân bằng hóa học
1. Phản ứng một chiều
- Là phản ứng chỉ xảy ra một chiều từ trái sang phải.
* Ví dụ: KClO3 2KCl + 3O2
- Trong phương trình hóa học của phản ứng một chiều, người ta dùng một mũi tên chỉ chiều phản ứng.
2. Phản ứng thuận nghịch
- Là những phản ứng xảy ra theo hai chiều trái ngược nhau trong cùng điều kiện.
* Ví dụ: Cl2 + H2O ⇌ HCl + HClO
- Chiều mũi tên từ trái sang phải là chiều phản ứng thuận.
- Chiều mũi tên từ phải sang trái là chiều phản ứng nghịch.
- Trong phương trình hóa học của phản ứng thuận nghịch, người ta dùng hai mũi tên ngược chiều nhau.
3. Cân bằng hóa học
- Là trạng thái của phản ứng thuận nghịch, ở đó, trong cùng một đơn vị thời gian có bao nhiêu phân tử chất sản phẩm được hình thành từ những chất ban đầu thì có bấy nhiêu phân tử chất sản phẩm phản ứng với nhau để tạo thành chất ban đầu.
⇒ Trạng thái này của phản ứng thuận nghịch được gọi là cân bằng hóa học.
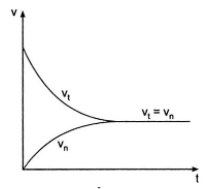 - Kết luận: Cân bằng hóa học là trạng thái của phản ứng thuận nghịch khi tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
- Kết luận: Cân bằng hóa học là trạng thái của phản ứng thuận nghịch khi tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
II. Sự chuyển dịch cân bằng
- Sự chuyển dịch cân bằng hóa học là sự di chuyển từ trạng thái cân bằng này sang trạng thái cân bằng khác do tác động của các yếu tố từ bên ngoài lên cân bằng.
III. Các yếu tố ảnh hưởng đến cân bằng hóa học
1. Ảnh hưởng của nồng độ
- Khi tăng hoặc giảm nồng độ một chất trong cân bằng thì cân bằng bao giờ cũng chuyển dịch theo chiều làm giảm tác động của việc tăng hoặc giảm nồng độ của chất đó.
> Lưu ý: Chất rắn không làm ảnh hưởng đến cân bằng của hệ.
2. Ảnh hưởng của áp suất
- Khi tăng hoặc giảm áp suất chung của hệ cân bằng thì cân bằng bao giờ cũng chuyển dịch theo chiều làm giảm tác động của việc tăng hoặc giảm áp suất đó.
> Lưu ý: Khi số mol khí ở 2 vế bằng nhau (hoặc phản ứng không có chất khí) thì áp suất không ảnh hưởng đến cân bằng.
3. Ảnh hưởng của nhiệt độ
* Phản ứng thu nhiệt và phản ứng tỏa nhiệt:
- Phản ứng thu nhiệt là phản ứng lấy thêm năng lượng để tạo sản phẩm. Kí hiệu ΔH > 0.
- Phản ứng tỏa nhiệt là phản ứng mất bớt năng lượng. Kí hiệu ΔH < 0.
* Khi tăng nhiệt độ, cân bằng chuyển dịch theo chiều phản ứng thu nhiệt (giảm tác động tăng nhiệt độ). Khi giảm nhiệt độ, cân bằng chuyển dịch theo chiều phản ứng tỏa nhiệt (giảm tác động giảm nhiệt độ).
* Nguyên lí chuyển dịch cân bằng Le Chatelier (Lơ Sa-tơ-li-ê): Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu một tác động từ bên ngoài như biến đổi nồng độ, áp suất, nhiệt độ thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động bên ngoài đó.
4. Vai trò của chất xúc tác
- Chất xúc tác không ảnh hưởng đến cân bằng hóa học.
- Vai trò chất xúc tác là làm tăng tốc độ phản ứng thuận và phản ứng nghịch với số lần bằng nhau.
- Khi chưa cân bằng thì chất xúc tác làm cho cân bằng thiết lập nhanh hơn.
IV. Ý nghĩa của tốc độ phản ứng và cân bằng hóa học trong sản xuất hóa học
- Dựa vào những yếu tố ảnh hưởng đến tốc độ phản ứng hóa học và cân bằng hóa học để chọn lọc nâng cao hiệu suất trong sản xuất hóa học.
* Ví dụ: trong sản xuất H2SO4 phải dùng trục tiếp phản ứng:
2SO2 (k) + O2 (k) ⇌ 2SO3 ∆H = -198kJ < 0.
- Phản ứng tỏa nhiệt, nên khi tăng nhiệt độ cân bằng chuyển theo chiều nghịch giảm hiệu suất phản ứng. Để cân bằng chuyển dịch theo chiều thuận người ta tăng nồng độ oxi (dùng lượng dư không khí).
Trên đây KhoiA.Vn đã giới thiệu với các em về Cân bằng hóa học là gì? Các yếu tố ảnh hướng tới sự cân bằng hóa học, nguyên lý Le Chatelier. Hy vọng bài viết giúp các em hiểu rõ hơn. Nếu có câu hỏi hay góp ý các em hãy để lại bình luận dưới bài viết, chúc các em thành công.
Đánh giá & nhận xét
- Tìm m để đường thẳng tiếp xúc với đường tròn Toán 10 - Hỏi nhanh đáp gọn
- Đơn vị Micro, Nano, Pico? Bảng mẫu đơn vị về ước số và bội số trong SI? Hỏi đáp môn Vật lí
- Hệ đơn vị SI là gì? 7 đơn vị cơ bản của hệ SI? Hỏi nhanh đáp gọn môn Vật lí
- Giải hệ phương trình bằng quy tắc Cramer, Phương pháp định thức Cramer lớp 10
- Phương trình bậc 2 có đúng 1 nghiệm dương khi nào? Điều kiện PT bậc 2 có đúng 1 nghiệm dương - Toán lớp 10
- Giải Vật lí 10 trang 92 Chân trời Sáng tạo
- Giải Vật lí 10 trang 91 Chân trời Sáng tạo
- Giải Vật lí 10 trang 90 Chân trời Sáng tạo
- Giải Vật lí 10 trang 89 Chân trời Sáng tạo
- Giải Vật lí 10 trang 88 Chân trời Sáng tạo


































