Tính chất hoá học của Photpho, Tính chất vật lí của photpho, sản xuất và ứng dụng photpho - Hoá 11 bài 10
Photpho (ký hiệu là P) thường gặp 2 dạng phổ biến là P đỏ và P trắng, phần lớn photpho được dùng để sản xuất axit photphoric H3PO4, phần còn lại chủ yếu dùng trong sản xuất diêm,...
Nội dung bài viết này sẽ giúp các em biết tính chất hoá học của photpho (P), photpho có tính chất vật lý gì đặc trưng? Photpho được điều chế như thế nào và có ứng dụng gì trong đời sống thực tế?
I. Cấu tạo nguyên tử và tính chất vật lý của photpho
1. Cấu hình nguyên tử Photpho
a) Sơ lược về photpho trong bảng tuần hoàn
- Photpho ô thứ 15 nhóm VA chu kỳ 3
- Cấu hình electron: 1s22s22p63s23p3
- Khối lượng nguyên tử: 31
b) Cấu tạo phân tử Photpho
- Photpho trắng có kiểu mạng phân tử còn Photpho đỏ có cấu trúc kiểu polime
- Do có 5 electron ở lớp ngoài cùng nên trong các hợp chất hoá trị của photpho có thể là 5 hoặc 3.
2. Tính chất vật lý của Photpho
• Photpho thường gặp 2 dạng thù hình phổ biến là P đỏ và P trắng:
a) Photpho trắng (P trắng)
- Là chất rắn trong suốt, màu trắng hoặc vàng nhạt, giống sáp, có cấu trúc mạng tinh thể phân tử: ở các nút mạng là các phân tử hình tứ diện P4 liên kết với nhau bằng lực tương tác yếu. Do đó photpho trắng mềm dễ nóng chảy (t0nc = 44,10C)
- Photpho trắng không tan trong nước, nhưng tan nhiều trong các dung môi hữu cơ như benzen, cacbon đisunfua, ete, …; rất độc gây bỏng nặng khi rơi vào da.
- Photpho trắng bốc cháy trong không khí ở t0 > 400C, nên được bảo quản bằng cách ngâm trong nước.
- Ở nhiệt độ thường, photpho trắng phát quang màu lục nhạt trong bóng tối. Khi đun nóng đến 2500C không có không khí, photpho trắng chuyển dần thành photpho đỏ là dạng bền hơn.
b) Photpho đỏ (P đỏ)
- Là chất bột màu đỏ có cấu trúc polime nên khó nóng chảy và khó bay hơi hơn photpho trắng
- Photpho đỏ không tan trong các dung môi thông thường, dễ hút ẩm và chảy rữa.
- Photpho đỏ bền trong không khí ở nhiệt độ thường và không phát quang trong bóng tối. Nó chỉ bốc cháy ở t0 > 2500C.
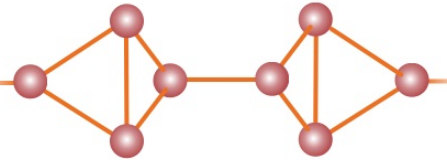
Cấu trúc polime của photpho đỏ
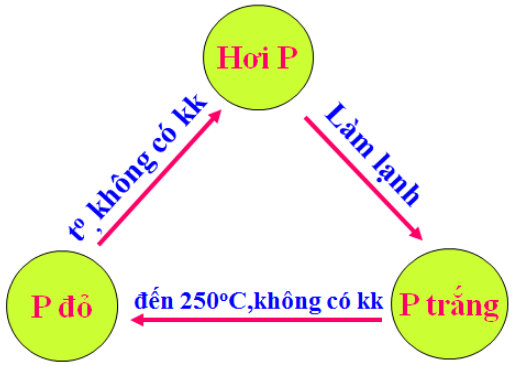
c) Chuyển hoá giữa Photpho trắng và đỏ
- Khi đun nóng không có không khí, photpho đỏ chuyển thành hơi, khi làm lạnh thì hơi của nó ngưng tụ lại thành photpho trắng.
II. Tính chất hoá học của Photpho
• Photpho có thể có các mức oxi hóa: -3, 0, +3, +5.
• Photpho hoạt động hóa học mạnh hơn N2 vì liên kết P - P kém bền hơn so với liên kết N ≡ N.
• P trắng hoạt động hơn P đỏ (vì P trắng có kiểu mạng phân tử còn P đỏ có cấu trúc kiểu polime).
1. Tính oxi hóa của Photpho
• P có phản ứng với nhiều kim loại → muối photphua:
2P + 3Mg → Mg3P2
• Các muối photphua bị thủy phân mạnh giải phóng photphin (PH3).
Ca3P2 + 6H2O → 2PH3 + 3Ca(OH)2
• Photphin là một khí không màu rất độc, có mùi tỏi, bốc cháy trong không khí ở nhiệt độ gần 1500C.
2PH3 + 4O2 → P2O5 + 3H2O
2. Tính khử của Photpho
• Phản ứng với phi kim: O2, halogen,...
4P + 3O2 → 2P2O3
4P + 5O2 → 2P2O5 (nếu O2 dư)
• P trắng phản ứng được ở ngay nhiệt độ thường và có hiện tượng phát quang hóa học; P đỏ chỉ phản ứng khi nhiệt độ > 2500C.
2P + 3Cl2 → 2PCl3
2P + 5Cl2 → 2PCl5
• Phản ứng với các chất oxi hóa khác
6P (đỏ) + 3KClO3 ![xrightarrow[]{t^{0}}](https://hayhochoi.vn/uploads/news/wyswyg/2019_03/1553913037el4ll7q6x8.gif) 3P2O5 + 5KCl (phản ứng xảy ra khi quẹt diêm)
3P2O5 + 5KCl (phản ứng xảy ra khi quẹt diêm)
6P (trắng) + 5K2Cr2O7 → 5K2O + 5Cr2O3 + 3P2O5
P + 5HNO3 → H3PO4 + 5NO2 + H2O
2P + 5H2SO4 đặc → 2H3PO4 + 3H2O + 5SO2
III. Điều chế và Ứng dụng của Photpho
1. Trạng thái tự nhiên của photpho
• Trong tự nhiên chỉ tồn tại ở dạng hợp chất. Hai khoáng vật chính là apatit 3Ca3(PO4)2.CaF2 và photphorit Ca3(PO4)2.
2. Điều chế Photpho
• Điều chế photpho trong công nghiệp
- Photpho được sản xuất bằng cách nung hỗn hợp quặng photphorit, cát và than cốc ở trong lò điện:
Ca3(PO4)2 + 3SiO2 + 5C ![]() 3CaSiO3 + 2P + 5CO (lò điện ở 15000C)
3CaSiO3 + 2P + 5CO (lò điện ở 15000C)
3. Ứng dụng của Photpho
• Phần lớn photpho được dùng để sản xuất axit photphoric H3PO4, phần còn lại chủ yếu dùng trong sản xuất diêm.
• Ngoài ra, Photpho trắng có ứng dụng trong quân sự là phần lớn bởi tính dễ cháy, tạo màn khói, sương độc. Phốtpho trắng cháy ngay ở nhiệt độ thường khi tiếp xúc với Oxi và tạo ra ngọn lửa rất độc với con người.
• Photpho đỏ không cháy ở nhiệt độ thường và thường được sử dụng làm hóa chất trong công nghiệp và trồng trọt.
Trên đây KhoiA.Vn đã giới thiệu với các em về Tính chất hoá học tính chất vật lí của photpho? Photpho được điều chế như thế nào và có ứng dụng gì trong đời sống thực tế? trong SGK Hóa học 11 nội dung bài 10. Hy vọng bài viết giúp các em hiểu rõ hơn. Nếu có câu hỏi hay góp ý các em hãy để lại bình luận dưới bài viết, chúc các em thành công.
• Xem hướng dẫn giải bài tập Hoá học 11
Đánh giá & nhận xét
- Bài 2 trang 86 SGK Vật lí 11 Chân trời sáng tạo
- Bài 1 trang 86 SGK Vật lí 11 Chân trời sáng tạo
- Bài 3 trang 79 SGK Vật lí 11 Chân trời sáng tạo
- Bài 2 trang 79 SGK Vật lí 11 Chân trời sáng tạo
- Bài 1 trang 79 SGK Vật lí 11 Chân trời sáng tạo
- Bài 3 trang 72 SGK Vật lí 11 Chân trời sáng tạo
- Bài 2 trang 72 SGK Vật lí 11 Chân trời sáng tạo
- Bài 1 trang 72 SGK Vật lí 11 Chân trời sáng tạo
- Bài 2 trang 61 SGK Vật lí 11 Chân trời sáng tạo
- Bài 1 trang 61 SGK Vật lí 11 Chân trời sáng tạo


































