Tính chất vật lý, Tính chất hóa học, Điều chế và Ứng dụng của Anken - Hóa 11 bài 29
Anken hay olefin có công thức phân tử chung là CnH2n (n≥2) thường được dùng làm nguyên liệu cho nhiều quá trình sản xuất hóa học. Etilen, propilen, butilen, được dùng làm chất đầu tổng hợp các polime có nhiều ứng dụng.
Nội dung bài viết này sẽ giúp các em biết cấu tạo phân tử, cách gọi tên, tính chất vật lý, tính chất hóa học của ANKEN, cách điều chế và ứng dụng của anken. Đồng thời biết phân biệt anken với ankan bằng phương pháp hóa học.
I. Đồng đẳng, đồng phân, danh pháp anken
1. Dãy đồng đẳng của anken
- Etilen (CH2 = CH2) và các chất tiếp theo có công thức phân tử C3H6, C4H8, C5H10,... có tính chất tương tự etilen lập thành dãy đồng đẳng có công thức phân tử chung CnH2n (n ≥ 2) được gọi là anken hay olefin.
2. Đồng phân anken
a) Đồng phân cấu tạo
- Anken từ C4H8 trở đi có đồng phân cấu tạo mạch cacbon và vị trí nối đôi.
b) Đồng phân hình học
- Nếu mỗi C mang liên kết đôi dính với 2 nhóm nguyên tử khác nhau thì sẽ có 2 cách phân bố không gian khác nhau là đồng phân cis và trans.
- Cách đọc tên đồng phân hình học: ghi tiền tố cis- trans- trước tên gọi anken
3. Danh pháp
a) Tên thông thường của anken
- Một số ít anken có tên thông thường, xuất phát từ tên ankan có cùng số nguyên tử cacbon bằng cách đổi đuôi -an thành -ilen.
* Ví dụ: etilen C2H4; propilen C3H6; butilen C4H8.
b) Tên thay thế của anken
- Tên thay thế: Số chỉ vị trí nhánh – Tên nhánh + Tên mạch chính – Số chỉ vị trí liên kết đôi – en
* Ví dụ: CH2=CH-CH2-CH3: But–1–en.
CH3-CH=CH-CH3: But–2–en.
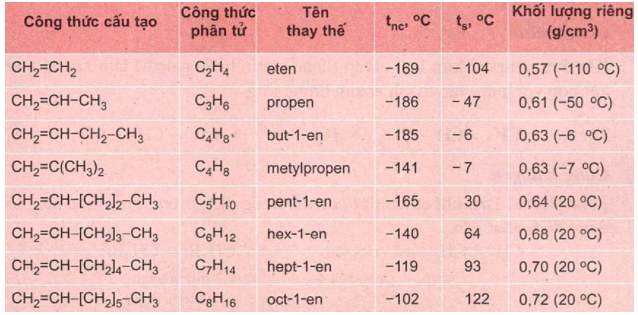 Tên thay thế và một vài thông số vật lý của một số anken
Tên thay thế và một vài thông số vật lý của một số anken
II. Tính chất vật lý của anken
- Ở điều kiện thường, các anken từ C2H4 đến C4H8 là chất khí; từ C5H10 trở đi là chất lỏng hoặc chất rắn.
- Nhiệt độ nóng chảy, nhiệt độ sôi và khối lượng riêng của các anken tăng dần theo chiều tăng của phân tử khối.
- Các anken đều nhẹ hơn nước (D < 1 g/cm3) và không tan trong nước.
III. Tính chất hóa học của anken
Trong phân tử anken có 1 ππ kém bền nên có phản ứng đặc trưng là phản ứng cộng.
1. Phản ứng cộng của anken
a) Phản ứng Cộng hiđro của anken
- Khi đun nóng có kim loại niken (hoặc platin hoặc palađi) làm xúc tác, anken kết hợp với hiđro tạo thành ankan tương ứng.
CnH2n + H2 CnH2n+2
b) Phản ứng cộng halogen của anken
- Etilen và các đồng đẳng của etilen đều làm mất màu dung dịch brom.
CnH2n + X2 CnH2nX2
c) Phản ứng cộng HX (X là OH, Cl, Br,...)
- Các anken cũng tham gia phản ứng cộng với nước, với hiđro halogenua (HCl, HBr, HI), với các axit mạnh.
CH2=CH2 + HOH CH3-CH2-OH
CH2=CH2 + HBr → CH3-CH2-Br
- Các anken có cấu tạo phân tử không đối xứng khi tác dụng với HX có thể sinh ra hỗn hợp hai sản phẩm.
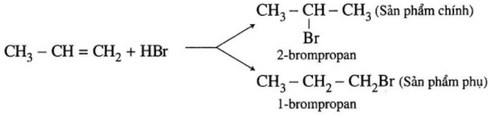
- Quy tắc cộng Mac-côp-nhi-côp (1838-1904): Trong phản ứng cộng HX vào liên kết đôi, nguyên tử H (hay phần mang điện dương) chủ yếu cộng vào nguyên tử cacbon bậc thấp hơn (có nhiều H hơn), còn nguyên tử hay nhóm nguyên tử X (phần mang điện âm) cộng vào nguyên tử cacbon bậc cao hơn (có ít H hơn).
2. Phản ứng trùng hợp
- Ở nhiệt độ cao, áp suất cao và có chất xúc tác thích hợp, các phân tử anken có thể kết hợp với nhau tạo thành những phân tử có mạch rất dài và phân tử khối lớn.
* Ví dụ: 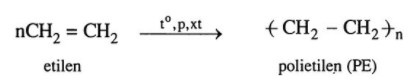
- Phản ứng trùng hợp là quá trình cộng hợp liên tiếp nhiều phân tử nhỏ giống nhau hoặc tương tự nhau tạo thành phân tử lớn gọi là polime.
- Số lượng mắt xích trong một phân tử polime gọi là hệ số trùng hợp, kí hiệu n.
3. Phản ứng oxi hóa
a) Phản ứng oxi hóa hoàn toàn
- Khi bị đốt với oxi, etilen và các đồng đẳng đều cháy và tỏa nhiều nhiệt.
> Nhận xét: Đốt anken thu được nCO2 = nH2O
b) Phản ứng oxi hóa không hoàn toàn
- Anken làm mất màu dung dịch KMnO4 (phản ứng được dùng để nhận ra sự có mặt của liên kết đôi) và bị oxi hóa không hoàn toàn thành hợp chất điol.
3CH2=CH2 + 4H2O + 2KMnO4 → 3HO–CH2–CH2–OH + 2MnO2↓(nâu đen) + 2KOH
- Phản ứng này dùng để phân biệt anken với ankan.
IV. Điều chế anken
1. Điều chế anken trong phòng thí nghiệm
- Etilen được điều chế từ ancol etylic (môi trường H2SO4 đặc 1700C):
2. Điều chế anken trong công nghiệp
Các anken được điều chế từ ankan:
V. Ứng dụng của anken
- Các anken và dẫn xuất của anken là nguyên liệu cho nhiều quá trình sản xuất hóa học.
- Etilen, propilen, butilen được dùng làm chất đầu tổng hợp các polime có nhiều ứng dụng.
Trên đây KhoiA.Vn đã giới thiệu với các em về Tính chất vật lý, Tính chất hóa học, Điều chế và Ứng dụng của Anken. Hy vọng bài viết giúp các em hiểu rõ hơn. Nếu có câu hỏi hay góp ý các em hãy để lại bình luận dưới bài viết, chúc các em thành công.
Đánh giá & nhận xét
- Bài 2 trang 86 SGK Vật lí 11 Chân trời sáng tạo
- Bài 1 trang 86 SGK Vật lí 11 Chân trời sáng tạo
- Bài 3 trang 79 SGK Vật lí 11 Chân trời sáng tạo
- Bài 2 trang 79 SGK Vật lí 11 Chân trời sáng tạo
- Bài 1 trang 79 SGK Vật lí 11 Chân trời sáng tạo
- Bài 3 trang 72 SGK Vật lí 11 Chân trời sáng tạo
- Bài 2 trang 72 SGK Vật lí 11 Chân trời sáng tạo
- Bài 1 trang 72 SGK Vật lí 11 Chân trời sáng tạo
- Bài 2 trang 61 SGK Vật lí 11 Chân trời sáng tạo
- Bài 1 trang 61 SGK Vật lí 11 Chân trời sáng tạo


































